Anvisa autoriza fase 3 de estudo com medicamento contra covid-19

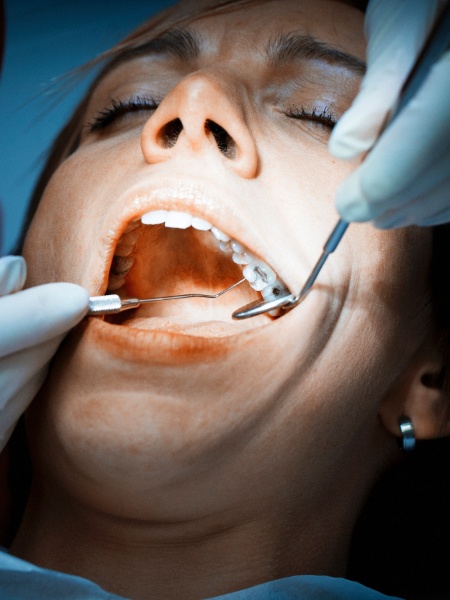
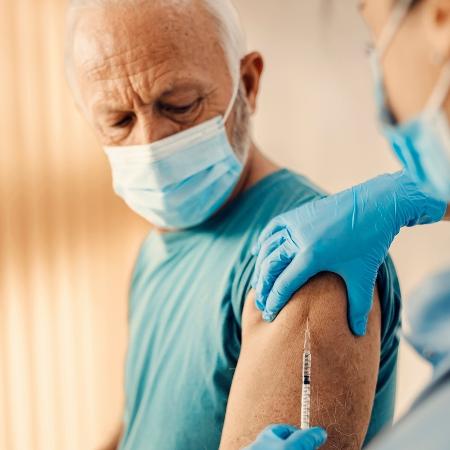
A farmacêutica Biomm informou, em fato relevante na segunda-feira, 2, que recebeu autorização da Agência Nacional de Vigilância Sanitária (Anvisa) para iniciar o estudo clínico de fase 3 do anticorpo monoclonal leronlimab no Brasil contra a covid-19.
De acordo com o CEO da companhia, Heraldo Marchezini, os testes ajudam a esclarecer as informações necessárias para encontrar uma nova alternativa no tratamento da covid-19 em pacientes internados.
A investigação será realizada em 35 centros de pesquisa com 612 pacientes que se encontram hospitalizados e com necessidade de suporte para oxigenação. O objetivo do medicamento, segundo a farmacêutica, é impedir que a doença evolua para um caso mais grave, com necessidade de ventilação mecânica invasiva.
O leronlimab age para prevenir uma resposta excessiva do sistema imunológico de pacientes infectados com o novo coronavírus, reduzindo a superprodução de citocinas inflamatórias, também conhecidas como "tempestade de citocinas". "Esta tempestade inflamatória, que agrava a condição clínica significativamente, pode, muitas vezes, levar o paciente a óbito", declara a Biomm.
O ensaio clínico será conduzido pela Academic Research Organization (ARO) do Hospital Israelita Albert Einstein (HIAE), em colaboração com a CytoDyn, empresa americana responsável pelo desenvolvimento do medicamento, e a Biomm, parceira exclusiva para a comercialização do leronlimab no Brasil.









ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.