Família cria plano para enfrentar a doença rara do filho

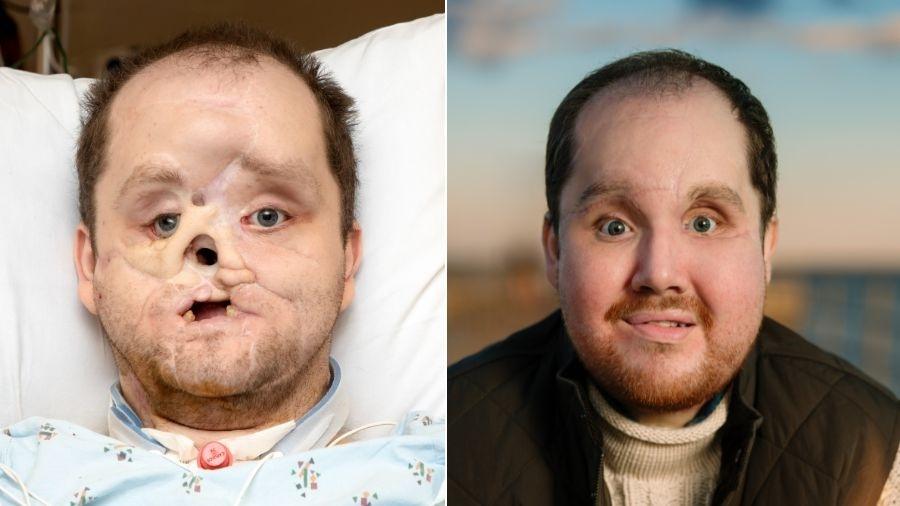
Uma década atrás, quando seu filho Bertrand ainda era um bebê, Matthew Might e a esposa, Cristina, perceberam que havia algo horrivelmente errado.
Quando ele chorava, os olhos permaneciam secos; a falta de lágrimas danificou as córneas e ameaçava causar cegueira. Por fim, ele sofreu convulsões, um transtorno de movimento e atraso agudo de desenvolvimento.
Veja também:
- Thais Fersoza tem espécie de tumor benigno no joelho; entenda a doença
- Cientistas descobrem proteína que pode prevenir esclerose
- Estresse aumenta em 36% os riscos de desenvolver doenças autoimunes
Demorou quatro anos para descobrirem o problema: Bertrand herdara duas mutações do gene NGLY1 que desempenha um papel decisivo na reciclagem do "lixo celular". Aquilo significava que as células da criança estavam se afogando no próprio lixo.
Por fim, Matthew Might encontrou cerca de 60 pessoas com essa mutação. Ele descobriu um tratamento para o problema – um efeito colateral involuntário do antiácido de venda livre Prevacid – e começou a trabalhar com uma empresa para produzir uma versão mais forte da medicação.
Agora diretor do Instituto de Medicina de Precisão Hugh Kaul da Universidade do Alabama, campus de Birmingham, Estados Unidos, ele começou a criar um roteiro para outras famílias confrontadas por doenças raras – aproximadamente dez por cento da população ou 30 milhões de norte-americanos.
O "Times" conversou com Might sobre os desafios para encontrar tratamentos para essas doenças e sobre as experiências de sua família com o filho. A conversa abaixo foi editada e condensada.
P: Foi extraordinário o que conseguiu fazer por seu filho – encontrar outros pacientes e um remédio no qual agora trabalha para tornar mais eficaz?
R: No momento, parece ser um evento raro. Contudo, eu não acho que continuará sendo incomum de agora em diante.
P: Por que é relativamente fácil encontrar tratamento para algumas doenças raras e para outras não?
R: Em todo caso que testamos até agora, achamos alguma coisa. Apenas estamos encontrando drogas existentes que já funcionam.
P: São drogas que já foram aprovadas para outros propósitos?
R: A readaptação é uma etapa central na abordagem de enfermidades raras e para evitar os custos elevados que acompanham o desenvolvimento de novas drogas. O melhor seria testar todos os remédios aprovados que existem.
P: Algumas doenças são especialmente adequadas para essa abordagem?
R: Epilepsias provocadas por canal iônico – epilepsias onde existe uma nítida origem eletrofisiológica. Elas ocupam o ponto ideal quando se trata de encontrar tratamentos. Elas são mais ou menos acessíveis com drogas. Muitas moléculas aprovadas as encontram casualmente, mesmo quando não é isso que estão tentando fazer.
P: Obviamente, não é tão fácil achar um tratamento para toda doença rara.
R: Existem grandes grupos de doenças que não são tão simples. Não tem como atingir diretamente a causa básica.
P: Esse tipo de medicina personalizada será o futuro para todos?
R: Medicina personalizada ou de precisão é sem dúvida o futuro – não apenas porque é o melhor tratamento, mas, em longo prazo, também reduzirá o custo. No fim das contas, ao fornecer a medicação correta para o paciente certo na hora certa, ela também ficará mais barata.
P: Já chegamos lá?
R: Acho que estamos em um ponto de inflexão. Os custos caíram a um ponto em que é razoável começar a fazer isso basicamente para todos. Um grupo farmacogenético que lhe dará a resposta para praticamente qualquer droga no mercado custa em torno de US$ 300. E você terá esse dado durante a vida do paciente. Em algum instante, iremos sequenciar todos no nascimento.
P: Conhecer uma falha genética que provoque uma doença basta para descobrir como tratá-la?
R: Agora existe uma lacuna entre o diagnóstico e a terapêutica. A genética ficou muito boa em dizer ao paciente o que ele tem, mas não o que fazer a seguir.
P: Esse é o foco do seu trabalho atual – propor um roteiro para outras famílias seguirem na busca de um tratamento?
R: Esse é meu objetivo de vida agora: sistematizar o processo inteiro de achar tratamentos, então é mais ciência focalizada do que arte. Uma das coisas que estou criando como parte do meu instituto na Universidade do Alabama é a infraestrutura necessária para levar um paciente do diagnóstico à terapia.
Esse é um território desconhecido para os médicos. Eles não estão acostumados a dizer: "O que deve fazer agora é uma experiência científica". Entretanto, no caso de muitas doenças raras, é justamente isso que se deve fazer.
P: Que tipos de experiências?
R: Pode ser construir um verme ou uma mosca e testá-la. Pode ser um exame químico, em que se começa testando compostos contra um modelo celular ou animal. Ou poderia ser um exame genético no qual se procure genes que interajam com o gene que promove a sua enfermidade.
Nós esboçamos um plano de pesquisa para eles e dissemos que este é o próximo passo; chegamos a colocá-los em contato com os pesquisadores corretos para dar esse próximo passo.
P: É realmente viável desenvolver tratamentos personalizados para uma família ou pequeno número de pessoas?
R: A partir do momento que se coloca as empresas e instituições em contato, de repente vemos uma mudança do desenvolvimento de drogas de um processo intransponível para algo ao alcance da mão para pacientes individuais ou fundações de pacientes.
P: As empresas veem interesse financeiro suficiente no desenvolvimento de uma droga que tratará apenas centenas de pacientes?
R: Já vi empresas se envolverem em doenças com número tremendamente pequeno de pacientes. Fundações de pacientes têm um grande papel a desempenhar em remover o risco da ciência em torno do desenvolvimento terapêutico. Caso o risco seja reduzido o suficiente, as empresas passam a participar.
P: Seu objetivo é achar tratamento para todas as sete mil doenças raras conhecidas?
R: Para as sete mil conhecidas agora, e quantas mais restarem a ser encontradas.
P: Isso é realista?
R: Realista ou não, há um imperativo moral para que o façamos. Então, atacaremos uma por vez. Aprendi que não ajuda muito se concentrar no que é possível ou realista. Concentre-se apenas no próximo passo, continue dando um novo passo e veja até onde consegue avançar.
P: E como Bertrand está agora, com 10 anos de idade?
R: Está muito feliz. Ele certamente tem problemas graves de desenvolvimento que serão difíceis de corrigir. Se tivéssemos interferido antes, ele poderia estar melhor agora. Estou mais otimista com a próxima geração de pacientes.
Eu procuro coisas como células-tronco e medicina regenerativa para ver se pode existir alguma forma de dar uma oportunidade a Bertrand que ele nunca teve antes. Existem vários próximos passos. Só estou começando.
SIGA O UOL VIVABEM NAS REDES SOCIAIS
Facebook - Instagram - YouTube








ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.