Teich cita remdesivir, mas com ressalva; o que já se sabe sobre o remédio?
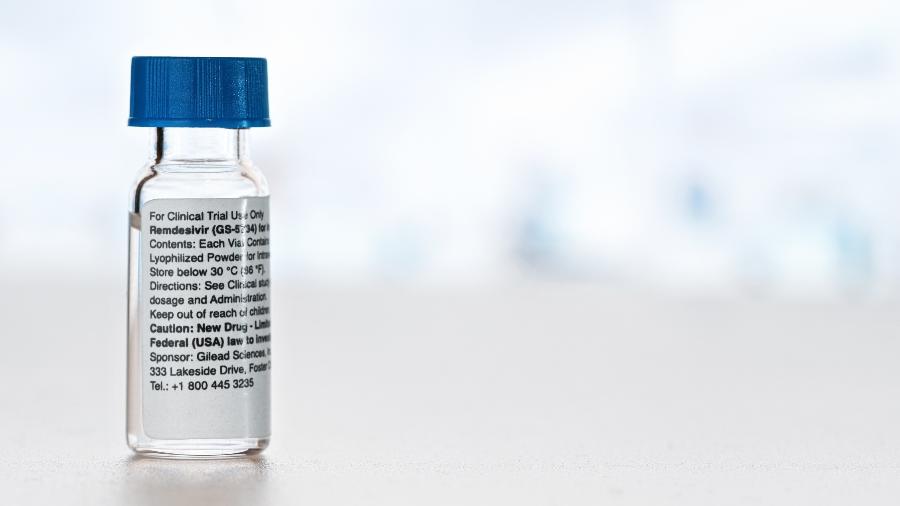
Durante entrevista à imprensa ontem (11), o ministro da Saúde Nelson Teich falou sobre o remdesivir, antiviral que vem apresentando bons resultados (embora discretos) no tratamento contra o novo coronavírus (Sars-CoV-2) em testes feitos nos EUA.
Por lá, o FDA (Food and Drug Administration) autorizou o uso do medicamento no dia 1º de maio para o tratamento de pacientes hospitalizados em estado grave com a covid-19.
"Baseado na totalidade das evidências científicas disponíveis, é razoável crer que o remdesivir possa ser efetivo no tratamento da covid-19 e que, quando usado sob as condições descritas nesta autorização, os conhecidos e potenciais benefícios superam os conhecidos e potenciais riscos da droga", afirma o documento do órgão norte-americano.
Embora concorde que o medicamento é "promissor", Teich fez ressalvas para o seu uso. "O ministério precisa ter um respaldo técnico em tudo o que ele recomenda. Quando a gente tiver algum estudo que comprove um benefício claro, vamos recomendar imediatamente. Fora isso, o ideal é que qualquer droga que pareça funcionar seja tratada em um estudo clínico para colher dados", afirmou.
Utilizado no tratamento de pacientes infectados com o vírus ebola, o remdesivir atualmente não possui registro nem é comercializado no Brasil. Também não há, por enquanto, estudos clínicos com ele sendo conduzidos no País.
Estudos apresentados são contraditórios
A autorização do remdesivir nos EUA já era esperada após a divulgação de resultados modestamente positivos do uso do medicamento. Os dados vieram de uma pesquisa conduzida pelo Instituto Nacional Americano de Saúde (NIH, na sigla em inglês), que considerou 1.063 pacientes nos EUA, na Europa e na Ásia. Os pacientes foram divididos entre os que receberam um tratamento com placebo e os que tomaram o remdesivir.
A análise preliminar do estudo indica que os pacientes tratados com o remédio se recuperavam cerca de quatro dias antes do que os outros. A taxa de mortalidade entre os que usaram a medicação também seria menor.
Mas cientistas do mundo todo ainda mantêm o ceticismo diante da notícia, já que, em outro estudo recente, feito por médicos chineses e publicado pelo periódico The Lancet, o antiviral teve pouco resultado entre os pacientes testados.
Quem está certo?
Desenvolvido para combater o ebola, o remdesivir já havia apresentado bons resultados quando utilizado para tratar pacientes vítimas dos coronavírus causadores da Sars e da Mers. No entanto, os estudos realizados com a Sars, em 2002, mostraram que, quanto mais se demorava para usar o remdesivir, menos eficaz ele era.
Isso poderia explicar porque os pacientes do estudo chinês não tiveram efeito benéfico com administração da droga, já que eles estavam em estado grave da covid-19.
Por isso, os cientistas aguardam resultados de outros testes em larga escala feitos com o remédio para elaborarem suas conclusões. Um deles é o estudo clínico Discovery, realizado pelo instituto de pesquisa francês Inserm desde 24 de março e que também leva em conta milhares de pessoas.
O infectologista brasileiro André Kalil, da Universidade de Nebraska Medical Center, lidera uma das pesquisas que estão sendo conduzidas com o antiviral. Para ele, novas evidências mostram que o medicamento é, sim, uma das melhores apostas no tratamento (e não na cura) dos pacientes infectados, mas ainda serão necessários novos estudos para que seu uso como padrão seja autorizado. "Estamos perto, mas ainda precisa de um tempo", disse, em entrevista à Folha de S.Paulo.
"Moderação é a palavra", diz especialista
Para o infectologista Ricardo Moura, do Hospital Sírio-Libanês (SP), a análise conduzida pelo NIH é uma das mais importantes, tanto pelo tamanho (com mais de mil pacientes) quanto pelos resultados.
"A pesquisa clínica revelou que os pacientes ou tiveram menos tempo de internação ou não precisaram de oxigenação suplementar, mas não mostrou nenhuma evidência sobre redução de mortalidade", explica.
No entanto, ainda são necessários mais dados para saber se a substância é de fato indicada para tratar os pacientes da covid-19.
"Como estamos aprendendo tudo agora enquanto a doença acontece, acredito que moderação é a palavra com relação a qualquer medicamento que apareça", afirma.
A médica Viviane Cordeiro Veiga, coordenadora de UTI da BP - A Beneficência Portuguesa de São Paulo, também concorda que, embora o estudo tenha apresentado resultados positivos discretos, ainda é cedo para tirar qualquer conclusão a respeito da substância. "Precisamos esperar o estudo ser finalizado e analisar sua qualidade.
Veiga, que faz parte da equipe da Coalização Covid Brasil (que está realizando alguns estudos com diversos medicamentos para o tratamento da covid-19 no País), lembra ainda que há outros medicamentos igualmente promissores em fase de teste. "Mas precisamos esperar os resultados dos estudos. E sabemos que, diante da situação atual, as pessoas e mesmo nós, que atuamos na linha de frente, queremos respostas o quanto antes", diz.
Anvisa já está em contato com fabricante
Buscando ter mais informações sobre o andamento dos testes, a Anvisa (Agência Nacional de Vigilância Sanitária) declarou que já está em contato com a Gilead, empresa que fabrica o remdesivir no exterior, para acompanhar a evolução dos estudos do medicamento no tratamento da covid-19.
O órgão informou ainda que deve realizar uma reunião com o fabricante em breve para verificar o interesse e a viabilidade do fornecimento do produto no Brasil.
A Gilead tem vários ensaios clínicos em andamento para o remdesivir, com dados iniciais esperados para serem divulgados nas próximas semanas. Caso o benefício do medicamento se comprove, a Anvisa possui mecanismos, como anuência de uso em programa assistencial e priorização de registro, para garantir o acesso rápido da medicação à população.
Por enquanto, o remdesivir não possui pedido de registro no país, nem solicitação de anuência em pesquisa clínica com o medicamento.
*Com informações de reportagem publicada em 02/05/2020.













ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.