Estudo confirma eficácia da Coronavac na fase 2 dos testes clínicos
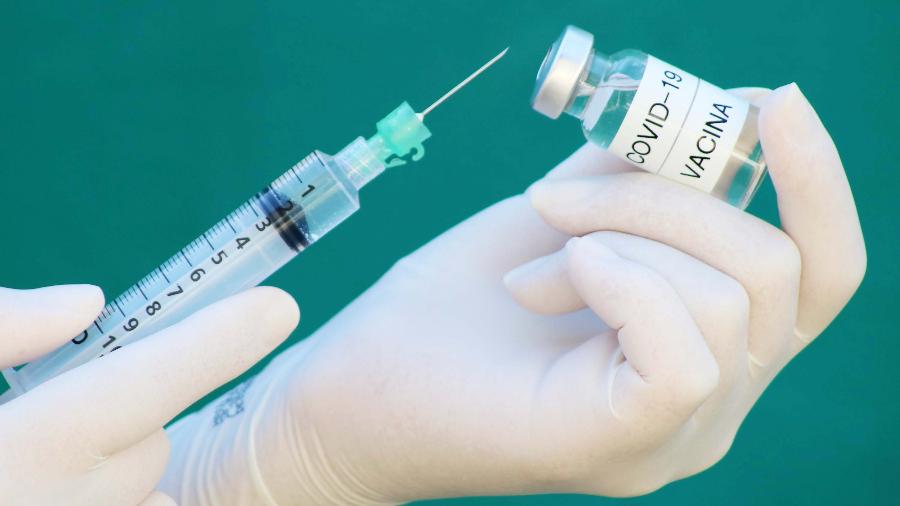
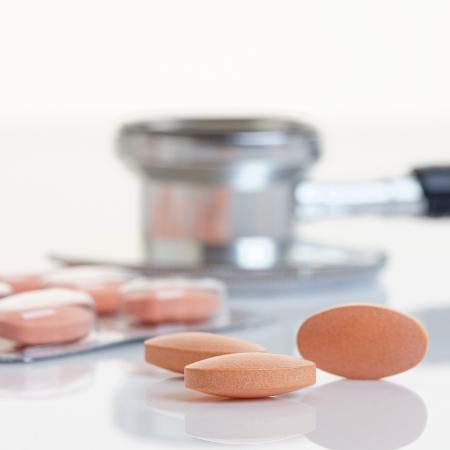
A vacina Coronavac se mostrou eficaz e segura, segundo estudo publicado nesta semana pela farmacêutica chinesa Sinovac Life Science. O trabalho analisou o comportamento de 600 voluntários vacinados na China durante a fase 2 dos testes clínicos. A vacina é desenvolvida pela Sinovac Life Science em parceria com o Instituto Butantan.
De acordo com o coordenador dos ensaios clínicos da vacina Coronavac e diretor médico de Pesquisa Clínica do Instituto Butantan, Ricardo Palacios, o produto é muito promissor e eficaz. "Os estudos feitos até agora, na China, demonstraram que mais de 90% dos voluntários que receberam as vacinas tiveram anticorpos capazes de neutralizar o coronavírus, isso é um diferencial", afirmou.
Segundo Palácios, os testes mostraram que entre duas e quatro semanas a pessoa está imunizada. "Duas semanas após a segunda dose as pessoas têm níveis de anticorpos capazes de neutralizar o vírus da covid-19", afirmou Palácios, em entrevista à Agência Brasil.
Cada voluntário recebeu duas doses, sendo metade a vacina propriamente dita e a outra metade placebo. De acordo com o que foi identificado nos estudos, não existe nenhuma preocupação com relação segurança da vacina utilizada nos voluntários. Dentre as principais reações está leve dor no local da aplicação, comum em outros tipos de vacina.
O laboratório asiático já realizou testes em cerca de mil voluntários na China, nas fases 1 e 2. Antes, o modelo experimental aplicado em macacos apresentou resultados expressivos em termos de resposta imune contra o coronavírus.
A farmacêutica forneceu ao Butantan as doses da vacina para a realização de testes clínicos de fase 3, a última fase, em voluntários no Brasil, com o objetivo de demonstrar sua eficácia e segurança. Os testes estão sendo feitos com os profissionais de saúde. Serão 9 mil voluntários da área de saúde em seis estados brasileiros: São Paulo, Brasília, Rio de Janeiro, Minas Gerais, Rio Grande do Sul e Paraná.
"A vacina é aplicada em voluntários, profissionais de saúde, que estão na linha de frente nos hospitais e que têm maior risco de contrair a doença, e isso é muito importante`, porque são profissionais que vão cuidar da gente, se ficarmos doentes", disse Palacios.
Caso a vacina seja aprovada, será realizada a transferência de tecnologia para produção em escala e fornecimento gratuito pelo SUS (Sistema Único de Saúde). Mas, antes, segundo Palacios, é preciso instalar a estrutura industrial para a produção.
"A parte de produção do vírus inativado propriamente dito é um pouco mais complexa, tem as adequações da própria estrutura, mas já começamos com essas adequações de equipamentos para, no término dos estudos, já estarmos com isso planejado". O passo seguinte será o registro do imunizante pela Anvisa (Agência Nacional de Vigilância Sanitária).












ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.