Fundo russo diz que enviou documentos para registro de vacina na Anvisa
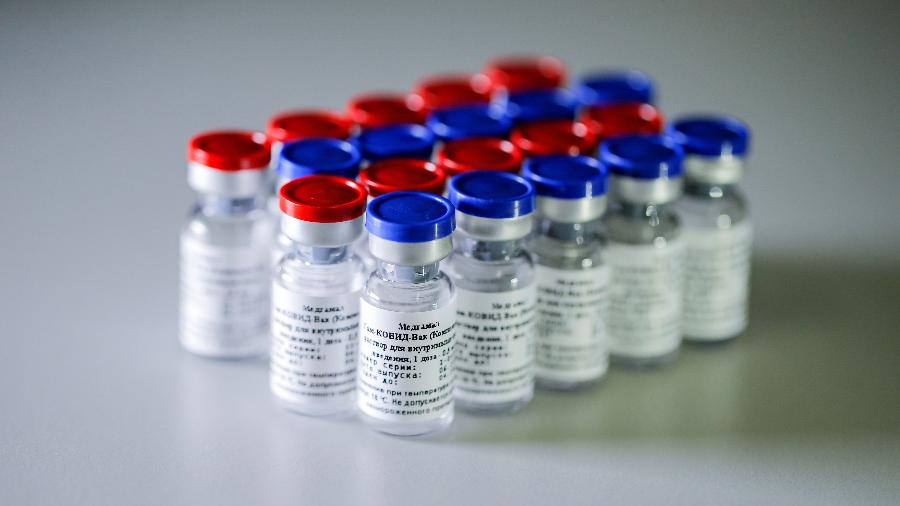
O Fundo de Investimentos Diretos da Rússia (RDIF), a empresa União Química Farmacêutica Nacional e o governo do Paraná anunciaram hoje (30) que foi realizada a pré-submissão à Anvisa (Agência Nacional de Vigilância Sanitária) dos documentos preliminares para registrar, em conformidade com os procedimentos regulatórios brasileiros, a vacina russa Sputnik V. Segundo comunicado do fundo, os documentos foram enviados ontem.
"O RDIF e a União Química, com o apoio do governo do Paraná, cooperam de forma proativa com a Agência Nacional de Vigilância Sanitária do Brasil, que tem desempenhado um papel fundamental e sensível para registrar, o quanto antes, a vacina Sputnik V no país. O registro permitirá passar à produção, bem como à distribuição da vacina no território brasileiro em breve", disse Kirill Dmitriev, presidente do fundo russo.
Em nota, a farmacêutica confirmou a informação. Já a Anvisa informou em comunicado oficial que não recebeu, até o momento, nenhum pedido de registro referente à vacina Sputnik V. O órgão ressaltou ainda que recebeu um e-mail do laboratório União Química sobre a apresentação apenas de documentos prévios. Os papéis foram enviados com um pedido para que a agência faça uma análise prévia, antes da apresentação formal do pedido de pesquisa.
A Anvisa disse também que as informações enviadas não são um pedido formal de autorização para a pesquisa e não são suficientes para a autorização da vacina aqui no Brasil. Na prática, a pesquisa não está autorizada e esse pedido ainda não foi feito pelo laboratório.
Ainda de acordo com o comunicado publicado pelo órgão, para uma vacina ser devidamente autorizada, ela precisa passar pelos processos de estudos clínicos e registro.
Primeira vacina registrada no mundo
Em 11 de agosto, a vacina Sputnik V, produzida pelo Centro Nacional de Pesquisas em Epidemiologia e Microbiologia Nikolay Gamaleya, recebeu um certificado de registro do Ministério da Saúde da Rússia, tornando-se a primeira vacina contra o coronavírus registrada no mundo.
Atualmente, o estudo pós-registro da vacina russa continua com a participação de 40 mil voluntários. Os primeiros resultados do estudo de pós-registro devem ser publicados em novembro de 2020.
Como parte do acordo de transferência da tecnologia entre o RDIF e a União Química, após devida autorização das autoridades sanitárias brasileiras será lançada a produção dos primeiros lotes da vacina por aqui.
Acordo com farmacêutica
A farmacêutica União Química informou no dia 23 de outubro que assinou acordo com o RDIF para produzir a vacina contra a covid-19 a partir da segunda quinzena de novembro. A empresa disse que firmou um acordo de confidencialidade que a impede de fornecer quaisquer detalhes técnicos ou científicos. O laboratório ainda precisa obter aprovação da Anvisa (Agência Nacional de Vigilância Sanitária) para a produção.
O acordo assinado pela União Química é o segundo para produção da vacina russa no Brasil. Além do Paraná, o governo da Bahia também assinou um acordo para conduzir testes clínicos de fase 3 e planeja comprar 50 milhões de doses. Não está claro, entretanto, quando esses testes podem começar.
Pedido à OMS
No dia 27 de outubro, a Rússia enviou à OMS (Organização Mundial da Saúde) um pedido de registro acelerado ("Uso Emergencial", EUL) e pré-qualificação da vacina Sputnik V, de acordo com o RDIF.
"Enviamos à OMS um pedido de registro rápido e pré-qualificação da vacina, o que permitirá que a Sputnik V seja incluído na lista de medicamentos que atendem aos principais padrões de qualidade, segurança e eficácia", disse Kirill Dmitriev, diretor do fundo, em comunicado.
O Programa de Pré-qualificação, organizado pela ONU e coordenado pela OMS, é, de fato, o único programa global de garantia de qualidade dos medicamentos. Se for pré-qualificada, a Sputnik V poderia ser incluída na lista de medicamentos que organizações e países usam para gerir sua aquisição em grande escala. (Com informações de Reuters e AFP)










ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.