Falta de documentos trava chegada de 4 milhões de doses da Covaxin

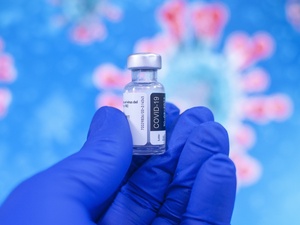
Quase duas semanas após a vacina Covaxin ter sido aprovada com restrições pela Anvisa (Agência Nacional de Vigilância Sanitária), uma questão burocrática tem travado a chegada ao Brasil de 4 milhões de doses da vacina indiana Covaxin contra a covid-19.
A Precisa Medicamentos, responsável pelo imunizante no país, e o Ministério da Saúde não têm se entendido quanto à licença de importação junto à Anvisa.
Questionada pelo UOL no início da semana, a empresa disse que, como o ministério é o importador, cabe à pasta pedir a licença de importação. Mas o ministério informou que ainda faltavam documentos para conseguir pedir a licença.
Documentação
Na terça-feira (15), a Precisa disse à reportagem que apenas após a emissão da licença é possível prever uma data de entrega dos 4 milhões de doses. "As doses estão prontas, aguardando a emissão da LI [licença de importação] para serem embarcadas", afirmou a empresa, que informa que as doses serão entregues "em uma única remessa".
O Ministério da Saúde, por sua vez, disse que a licença de importação está travada por causa da empresa. Em nota enviada ontem à reportagem, a pasta informou "que aguarda ajustes na documentação por parte da Precisa para emissão da licença de importação junto à Anvisa".
O ministério cita pontos como "certificado de liberação do lote, datas de fabricação, entre outros documentos", elencados na resolução da Anvisa sobre vacinas com autorização excepcional e temporária na pandemia do novo coronavírus, caso da Covaxin.
No final da tarde, a Precisa enviou uma nova mensagem reafirmando que os "documentos necessários foram enviados" e que a "licença foi aberta". O documento apresentado pela empresa é das 16h10, cerca de uma hora após a publicação da reportagem. "Agora cabe análise da Anvisa", diz a empresa.
De acordo com a Anvisa, ainda não houve recebimento do pedido de licença de importação, documento que deve ser apresentado pelo Ministério da Saúde, que também deve firmar um termo de compromisso sobre as condicionantes que a Anvisa colocou para o uso da Covaxin.
Como comparação, a CoronaVac pôde ser utilizada no mesmo dia em que foi aprovada pela agência, em 17 de janeiro. Já a vacina da AstraZeneca levou cerca de uma semana para começar a ser aplicada no país em razão principalmente da falta de doses do imunizante no Brasil, não por questão burocrática.
A falta de doses, e não de documentos, também causou o intervalo de cerca de um mês entre a aprovação da vacina da Pfizer no final de março e o início de sua aplicação no Brasil em maio.
Liberada com restrições
O Ministério da Saúde contratou 20 milhões de doses da Covaxin. No dia 4 de junho, a Anvisa aprovou a importação do imunizante, porém, com uso em condições controladas, liberando um quinto da quantidade contratada: 4 milhões.
A agência permitiu o uso apenas em adultos com idade entre 18 e 59 anos, excluindo grávidas, puérperas, lactantes e pessoas com comorbidades.
Os 4 milhões de doses poderão imunizar 2 milhões de pessoas. Seu esquema vacinal demanda a aplicação de duas does, com intervalo de 28 dias.
Em razão das incertezas sobre quando a Covaxin estará disponível no Brasil, ela consta nos cronogramas do ministério, porém, sem a indicação do momento da entrega. O mesmo acontece com a vacina Sputnik V.
Caso seja utilizado, o imunizante deve colaborar para acelerar o ritmo de vacinação no país, que têm estados projetando a aplicação de ao menos uma dose em toda sua população, no máximo, até outubro.









ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.