AstraZeneca afirma que coquetel anticovid é 83% eficaz após 6 meses
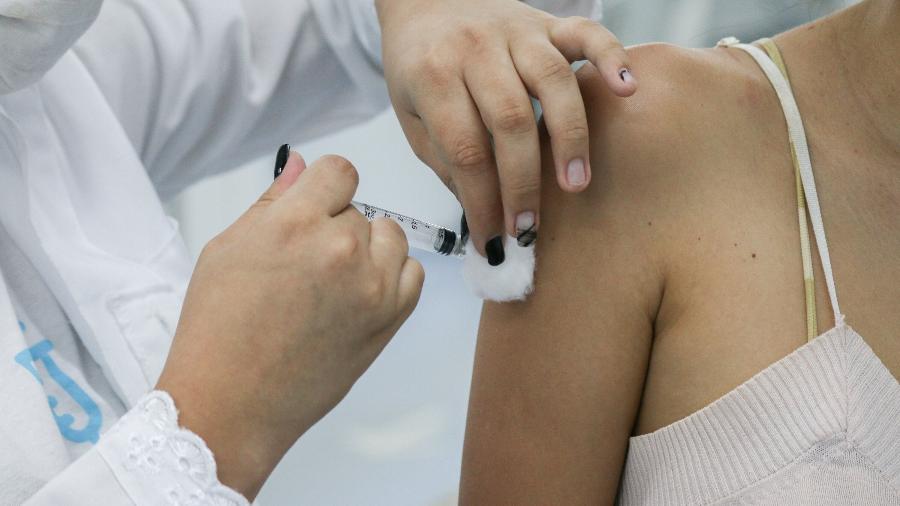
A AstraZeneca informou hoje que seu coquetel para a prevenção de covid-19 foi capaz de reduzir em 83% o risco de ocorrência sintomática da doença. Dentro do período de seis meses em que o produto foi analisado, não houve registros de casos graves ou óbitos por causa do coronavírus, disse a empresa.
Chamado de Evusheld (ou AZD7442), o coquetel combina cópias de dois anticorpos obtidos do plasma de pacientes convalescentes que se recuperaram de uma infecção com o coronavírus SARS-CoV-2. A terapia requer uma dose única de 300mg e é administrada por via intramuscular. O medicamento já havia demonstrado, em agosto, proteção de 77% contra casos sintomáticas da doença após três meses.
"O que é importante é que essa proteção em seis meses foi mantida nos participantes de alto risco e/ou imunocomprometidos, apesar do surto da variante Delta", disse, em nota, o autor do estudo, Hugh Montgomery, professor de medicina intensiva na University College London.
O medicamento também é eficaz na "profilaxia pós-exposição", ou seja, para evitar que uma pessoa recentemente infectada com o vírus desenvolva uma forma grave de covid-19. De acordo com outro ensaio clínico, a administração do AZD7442 por até três dias após o início de sintomas leves a moderados de covid-19 reduz o risco de casos graves ou morte em 88% em comparação com o placebo.
A AstraZeneca apresentou pedido de autorização de emergência para a Food and Drug Administration (FDA), a autoridade de saúde dos EUA. A Agência Europeia de Medicamentos (EMA) iniciou procedimento de avaliação em meados de outubro de dados contínuos sobre o Evusheld.
A EMA anunciou na semana passada a autorização de comercialização de dois produtos de anticorpos monoclonais para o tratamento de covid-19: a terapia ronapreve, desenvolvida pela empresa norte-americana de biotecnologia Regeneron em parceria com o laboratório suíço Roche; e a Regkirona, do laboratório Celltrion. A agência europeia já havia aprovado o remdesivir, da Gilead, em 2020.
O Regen-Cov (combinação de casirivimabe e imdevimabe), da Regeneron, tem aprovação para uso emergencial no Brasil. Estudo publicado na revista New England Journal of Medicine mostrou que o medicamento conseguiu reduzir casos de covid-19 em moradores de uma mesma casa em que havia pessoas infectadas com a doença. A droga também foi capaz de evitar hospitalização e mortes em pessoas com risco de desenvolvimento grave da doença.
Os anticorpos monoclonais desenvolvidos pela farmacêutica Eli Lilly conseguiram reduzir em até 70% o risco de hospitalizações e mortes por covid —a combinação de eanlanivimabe e etesevimabe também tem aprovação da Anvisa (Agência Nacional de Vigilância Sanitária).
O regdanvimabe, anticorpo monoclonal da Celltrion Healthcares, e o sotrovimabe, medicamento biológico da GSK, têm autorização para uso emergencial pela Anvisa. Ambos demonstraram reduções no risco de progressão da covid-19 em pessoas com 12 anos de idade ou mais.









ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.