Anvisa autoriza pesquisa com vacina tetravalente para gripe influenza
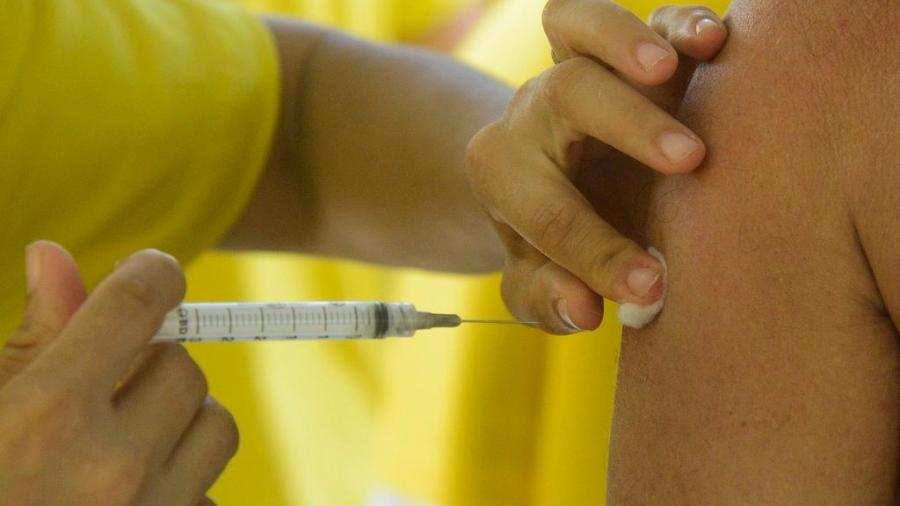
A Anvisa publicou, nesta quinta-feira (16), a autorização para o início do ensaio clínico fase 3 da vacina para a gripe influenza tetravalente (fragmentada e inativada) QIV-IB, desenvolvida pelo Instituto Butantan, de São Paulo.
O estudo pretende avaliar a imunogenicidade e segurança da vacina em lactentes e crianças de seis a 35 meses. Segundo a agência, a diferença entre o ensaio clínico aprovado nesta quinta-feira (FLQ-02-IB) e o anterior (FLQ-01-IB), de fevereiro, é a idade dos participantes.
Enquanto no primeiro os participantes teriam de ter três anos ou mais de idade, no ensaio clínico aprovado agora (FLQ-02-IB) serão incluídos participantes entre seis e 35 meses, além da dose da vacina ajustada para a idade.
O processo de produção da vacina tetravalente é semelhante ao da trivalente (fragmentada e inativada) do Instituto Butantan (TIV-IB), que já é utilizada nas campanhas nacionais de vacinação contra a gripe influenza, do Programa Nacional de Imunizações do Ministério da Saúde.
Enquanto uma das vacinas trivalentes contém o vírus B (linhagem Yamagata - TIV-Y-IB) e a outra tem o vírus influenza B (linhagem Victoria - TIV-V-IB), a vacina tetravalente possui as duas cepas da linhagem B na mesma formulação.
"Dessa forma, espera-se obter uma vacina influenza tetravalente análoga à trivalente, mas com uma proteção adicional contra uma segunda cepa B, determinada sazonalmente pela OMS. A adição da segunda cepa B de influenza (quarta cepa na vacina) ocorreu na transição da vacina influenza sazonal bivalente para a trivalente, após a pandemia de influenza H1N1 em 2009", explicou a Anvisa.
Pesquisa
De acordo com o protocolo clínico, a ideia é incluir cerca de 1,9 mil participantes —entre 6 a 35 meses— em dez centros distribuídos entre São Paulo, Roraima, Sergipe e Pernambuco. O tempo da participação será de aproximadamente seis meses após esquema completo de vacinação, enquanto o total do tempo do estudo estimado será cerca de 12 meses.
Ensaios clínicos
Ensaios clínicos são os estudos de um novo medicamento, realizados em seres humanos. A fase clínica serve para demonstrar a segurança e eficácia do medicamento experimental para a indicação proposta.
Havendo a comprovação de que os benefícios superam os riscos, o remédio experimental poderá ser registrado pela Anvisa e disponibilizado no mercado brasileiro, desde que haja a solicitação por parte da empresa desenvolvedora/patrocinadora do desenvolvimento clínico.











ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.