'Cada dia importa', diz cientista que criou o 1º remédio para tratar AME
O recém-nascido aparenta ser saudável, mas há algo de errado. Os meses passam e o bebê é incapaz de ficar sentado ou andar e tem o corpo mais mole do que o normal. O diagnóstico demora, mas assusta seus pais quando finalmente chega: a doença da criança é grave, não tem cura e é degenerativa. Sua expectativa de vida, avisam os médicos, é de dois anos.
Há 20 anos, nascer com AME (amiotrofia muscular espinhal) era uma sentença de morte. Na última década, porém, o tratamento da rara doença genética passou por uma verdadeira revolução, com a chegada de três remédios capazes de mudar seu curso natural.
A AME afeta os neurônios motores, responsáveis por controlar o funcionamento dos músculos. A condição leva à perda dos movimentos de braços e pernas e favorece o desenvolvimento de problemas respiratórios que, em estágios mais graves, podem levar à morte na infância.
O cientista uruguaio-americano Adrian Krainer começou a estudar mecanismos associados à doença em 1999. Uma técnica criada por ele ao lado do pesquisador Frank Bennett tornou possível o desenvolvimento do Spinraza, o primeiro remédio capaz de impedir a evolução da AME. Comercializado desde 2016 pela farmacêutica Biogen e disponível no SUS a partir de 2019, a descoberta rendeu à dupla o prêmio da edição 2019 do Breakthrough, conhecido como Oscar da Ciência.
O lançamento do medicamento foi seguido pelo chegada de outros dois também voltados para o tratamento da AME: o Zolgensma (2019), da Novartis, e o Risdiplam (2020), da Roche.
Com indicações, formas de administração e mecanismos diferentes, os três remédios de alto custo têm o mesmo objetivo: permitir que o paciente volte a produzir a proteína necessária para a sobrevivência dos neurônios motores. Uma reportagem de UOL Prime publicada há alguns dias conta o que mudou na vida da primeira criança brasileira que recebeu um desses remédios.
A VivaBem, Krainer, que é geneticista do Laboratório Cold Spring Harbor, nos EUA, explicou como funcionam os diferentes medicamentos para a AME, falou sobre as dificuldades de acesso ao tratamento e encorajou o Brasil a investir no diagnóstico precoce da doença. Leia a entrevista completa abaixo:
VivaBem: Como funciona o Spinraza, remédio que você ajudou a desenvolver, e como estão as crianças que o receberam?
Adrian Kariner: A AME é causada por uma mutação no gene SMN1, que impede o organismo de produzir a proteína SMN, responsável por manter os neurônios motores vivos. Sem ela, a capacidade de locomoção é prejudicada.
O que o Spinraza faz é permitir que outro gene do nosso corpo, o SMN2, produza essa proteína da maneira adequada. O mecanismo de ação é parecido com o Risdiplam, que também estimula o SMN2 a fabricar a proteína em falta nos pacientes que têm a doença.
Hoje, há mais de 11 mil pessoas em mais de 50 países que já utilizaram o Spinraza. Podemos afirmar que o remédio salvou e melhorou vidas.
A extensão da melhoria é variável, depende de quão cedo eles tiveram acesso ao tratamento —algo que é crucial para os três medicamentos disponíveis para AME.
Isso porque as pessoas nascem com essa condição genética, mas o diagnóstico costuma vir algum tempo depois do nascimento, porque os sintomas não são necessariamente óbvios nos primeiros dias de vida. O que sabemos agora é que, se começarmos o tratamento antes do início dos sintomas, você pode, de certa maneira, prevenir a doença.
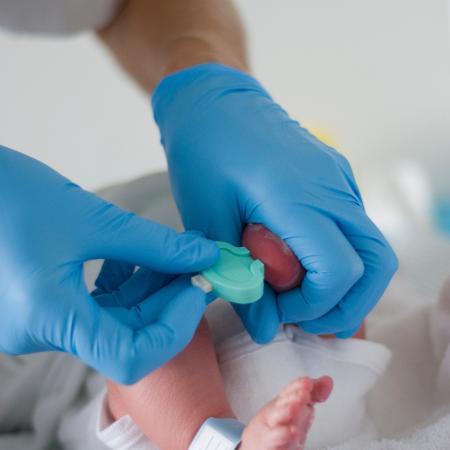
Nos EUA, por exemplo, há a triagem neonatal, então todo bebê que nasce é testado para uma série de doenças genéticas, incluindo a AME. E o que vemos é que, quando o paciente começa o tratamento nos primeiros dias de vida, praticamente não dá para dizer que ele tem a condição.
Alguns recém-nascidos que receberam Spinraza já estão com cinco anos, e mesmo que geneticamente tenham AME tipo 1, você quase não poderia dizer que eles têm a doença, porque é uma melhoria realmente dramática. Isso também acontece com os outros dois remédios. Então, a chave é começar o tratamento o mais cedo possível.
VivaBem: Crianças que receberam o tratamento mais tarde também apresentaram melhorias?
Adrian Krainer: Sim. Sem tratamento, o paciente com AME vai piorando com o passar do tempo. Se ele começar o tratamento mais tarde, em muitos casos o mínimo que vai acontecer é que ele não irá piorar e também é possível ver algumas melhorias com o auxílio da fisioterapia.
Mas é claro que a evolução não é tão boa quanto nos casos em que foi possível prevenir o aparecimento dos sintomas dando o remédio para o paciente desde recém-nascido.

VivaBem: Por que é tão importante receber o remédio o quanto antes?
Adrian Krainer: Nascemos com um certo número de neurônios motores, não produzimos durante a vida. Então, se alguma porção ou metade dos neurônios estiver morto, você só pode funcionar com aquilo que restou.
Os tratamentos permitem que os neurônios motores restantes permaneçam saudáveis e funcionem melhor, mas você não pode trazer de volta os que se foram. Por isso, ainda não dá para dizer que existe cura para a AME.
Trazer de volta os neurônios mortos seria medicina regenerativa e há pesquisas sobre isso em andamento, mas nada conclusivo. Por isso, quanto mais cedo você tratar, melhores serão os resultados. Cada dia importa.
VivaBem: Eu já ouvi algumas pessoas, principalmente famílias de crianças que têm AME, afirmarem que o Zolgensma seria "o melhor" remédio para tratar a doença. Qual a sua opinião sobre isso?
Adrian Krainer: Pessoalmente, acho que você não pode afirmar isso. Você pode apenas especular.
Obviamente, estive envolvido no desenvolvimento de um medicamento e trabalhei um pouco nos mecanismos de outro, então posso ter meus próprios vieses, mas a verdade é que se você quiser comparar terapias, teria que fazer um estudo duplo cego com o mesmo perfil de pacientes, e isso ainda não foi feito em nenhum lugar do mundo.
Você pode olhar para um ensaio clínico e olhar para outro ensaio clínico, mas se um dos testes envolveu pacientes mais novos, é claro que eles obterão resultados melhores, e vice-versa. Então, essas comparações são muito complicadas.
Além disso, existem alguns estudos em que os pacientes começaram com um medicamento e depois mudaram para outro, mas ainda não há estudos clínicos bem estruturados sobre esses casos. Existe alguma lógica pela qual você pode pensar em combinar dois ou três remédios, porque eles não funcionam exatamente da mesma maneira, mas isso obviamente é muito caro, porque os três medicamentos são muito caros.
O médico não pode dizer às famílias 'você deve usar este ou aquele medicamento', a menos que haja algum tipo específico de indicação. Geralmente, eles dizem 'esses são os medicamentos disponíveis, essas são as características de cada medicamento e vocês precisam decidir o que querem'.
As pessoas podem se sentir atraídas pelo Zolgensma pelo fato de ser uma dose única, mas a verdade é que ainda não podemos garantir que 20 anos depois, o remédio ainda estará funcionando em seu nível máximo. Também acho que, por ser mais caro, as pessoas têm expectativas mais altas sobre seus resultados.
VivaBem: Você ainda estuda a AME?
Adrian Krainer: Em relação à AME, meu laboratório fez um estudo recente em colaboração com Alberto Kornblihtt, da Universidad de Buenos Aires, em que procuramos combinar o Spinraza com um outro medicamento, chamado ácido valproico [remédio utilizado no tratamento da epilepsia].
O trabalho mostra que se combinarmos as duas drogas, nas células ou nos camundongos, podemos obter um pouco mais de proteína SMN.
Isso é evidente em laboratório, não estou recomendando que as pessoas façam isso nas clínicas, mas encorajamos os médicos a talvez realizarem ensaios clínicos de medicamentos para AME sozinhos versus em combinação com outros para demonstrar se há, de fato, um benefício. Agora, também estamos estudando a combinação de Spinraza com drogas moleculares como o Risdiplam.
VivaBem: Quais são suas perspectivas para o futuro do tratamento da AME?
Adrian Krainer: O que eu gostaria de ver, em primeiro lugar, é que todos no mundo tivessem acesso aos medicamentos.
Sei que eles são caros, mas cada país tem que descobrir uma maneira adequada de dar acesso às pessoas. Me incomoda muito ver pacientes que não têm condições de pagar um dos tratamentos e ficam sem acesso. Infelizmente, é um processo lento. Já faz sete anos desde a aprovação do primeiro medicamento, o Spinraza.
A triagem neonatal também é superimportante e geralmente também é um processo lento, mas eu encorajaria o Brasil e todos os países que ainda não incluíram a AME nesse exame a fazerem isso, porque vai ser bom para todos.
Essas crianças, quando crescerem, vão ser muito mais produtivas. Além disso, os enormes custos que as famílias com crianças com AME têm e o custo social decorrente do tratamento tardio também vão diminuir. Vale a pena investir em triagem neonatal. Não consigo pensar em nada mais importante do que isso.
Também precisamos apoiar pesquisas para obter ainda mais melhorias no tratamento, incluindo estudos que analisem a possibilidade de combinar diferentes terapias, medicina regenerativa e entender mecanismos que ainda não compreendemos inteiramente.
Sobre os remédios para AME
A principal diferença entre os três é a forma de administração.
O Spinraza, da Biogen, é aplicado a cada quatro meses, por meio de uma injeção na base da coluna vertebral.
O Risdiplam, da Roche, vem na forma de um líquido e deve ser tomado todos os dias.
Já o Zolgensma, da Novartis, é de aplicação única intravenosa e deve ser administrado até os dois anos de idade.


















Deixe seu comentário
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Leia as Regras de Uso do UOL.